- Trang chủ
- Sách y học
- Bài giảng huyết học và truyền máu
- Ghép tủy tế bào nguồn
Ghép tủy tế bào nguồn
Ghép tuỷ tế bào nguồn, nghĩa là truyền tế bào nguồn vào máu như truyền máu, nhưng không dùng màng lọc máu, truyền chậm và dùng kim luồn vào tĩnh mạch trung tâm.
Biên tập viên: Trần Tiến Phong
Đánh giá: Trần Trà My, Trần Phương Phương
Chuẩn bị tế bào nguồn cho ghép tuỷ
Nguồn cung cấp tế bào nguồn sinh máu (Sourse of Hemopoietic Progenitor Cells)
Tế bào có khả năng sinh máu (progenitors) đồng loài từ các người cho có cùng HLA (A, B, DR) hoặc từ chính bản thân bệnh nhân. Ở người sourse tế bào nguồn có thế phân lập từ các cơ quan sau đây (bảng).
Tuỷ xương.
Tế bào gan phôi.
Máu ngoại vi.
Máu cuống rốn.
Tuỷ xương bệnh nhân lơxêmi ở thời kỳ ổn định sau điều trị hoá chất, hoặc sau khi điều trị hoá chất có dùng chất kích thích GM, G - CSF.
Huy động tế bào nguồn từ tủy vào máu.
Nuôi cấy in-Situ (nuôi cấy dài ngày = longterm culture)
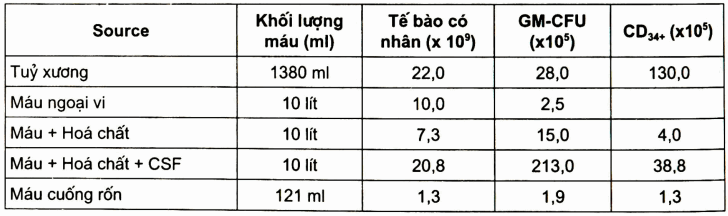
Bảng. Các Source của tế bào nguồn và khả năng cung cấp
Thu hoạch tế bào nguồn
Phân lập tế bào nguồn từ tuỷ:
Tuyển chọn người cho.
Chọc hút dịch tuỷ, thu khoảng 100 hoặc > 1000ml dịch tuỷ-chống đông.
Phân lập tế bào có nhân, tách tế bào nguồn.
Loại bỏ T lympho.
Bảo quản và sử dụng.
Phân lập tế bào nguồn từ máu ngoại vi:
Tuyển chọn người cho.
Phăn lập từ máu bằng phương pháp gạn tế bào nguổn sử dụng máy tự động.
Phân lập từ túi máu bằng ly tâm phân lớp.
Loại huyết tương.
Loại hồng cầu, loại T lympho, bảo quản ở -196°c và sử dụng.
Phân lập tế bào nguồn từ máu dây rốn trẻ sơ sinh:
Vô khuẩn trong quy trình thu gom, loại bớt HC, bảo quản ở -196°c và sử dụng.
Huy động tế bào nguồn:
Huy động tế bào nguồn bằng hoá chất kết hợp với chất kích thích G-CSF (Mobilization ofHSC by chemotherapy and G-CSF). Kỹ thuật này cho hiệu quả gấp 40 - 50 lần.
Hoá chất và chất kích thích thường dùng:
Cyclophosphamid, sau đó dùng G-CSF trên ngày thứ 4 - 6.
Thu hoạch tế bào progenitors: sau khi đã dùng G-CSF vào ngày 4 hoặc 5 thu hoạch tế bào nguồn bằng máy tự động.
Dùng chất kích thích đơn phương:
G - CSF, GM – CSF.
GF, IL-3..
Thrombopoietin.
Nuôi cấy in-situ: nuôi cấy clone bằng kỹ thuật insitu có chất kích thích.
Làm sạch tế bào nguổn
Loại T lympho:
Phương pháp miễn dịch:
Kỹ thuật sử dụng kháng thể đơn dòng chống T lympho (ATG).
E Rosette.
Miễn dịch hấp phụ (IM - adsoption).
Phương pháp dược lý: sử dụng các hoá chất + Cyclophosphamid.
Vincristin + Cyclosporin A.
Phương pháp sinh học:
Nuôi cấy dài ngày có chất kích thích T-Lympho + Hoạt hoá T lympho bằng IL-2, rồi loại bỏ tế bào T.
Loại tế bào lơxêmi sử dụng cho tự ghép tuỷ:
Nuôi cấy dài ngày: tế bào lơxêmi chết trước.
Đông tan: tế bào lơxêmi dễ bị ly giải hơn tế bào bình thường.
Loại bằng cảm ứng từ: làm sạch bằng phương pháp này có kết quả tốt, xong đắt tiền.
Bảo quản tế bào nguồn
Bảo quản bằng dung dịch DMSO (Dimethyl Sulíbside) 10% dùng dung dịch có 20% huyết tương của bản thân.
Làm lạnh: 1 - 5°c/l phút cho tói -30°c
Làm lạnh sâu: - 80°c
Âm 186°c trong nitơ lỏng (Liquid nitrogen)
Sử dụng tế bào nguồn bảo quản
Phá đông: nhanh, trong chậu nước ấm 37°c đến 40°c
Dung dịch tế bào được truyền bằng catheter qua tĩnh mạch thượng đòn.
Có thể thểm một bước trước khi truyền loại bỏ DMSO, giảm độc, nhưng thực chất không cần vì làm tổn thương tế bào nguồn.
Liều lượng (Dose) tế bào nguồn cần thiết cho ghép tuỷ:
Liều lượng dùng cho ghép đồng loại (Allograít) và ghép tự thân (autograft) như sau:

Bảng: Liều lượng dùng cho ghép đồng loại
Máu cuống rốn và ngân hàng máu rốn
Một nguồn cung cấp tế bào nguồn có giá trị.
Đặc điểm sinh học máu cuông rốn
Chỉ có dấu ấn CD34+, các dấu ấn khác đều chưa xuất hiện.
Phản ứng nhanh, nhậy với chất kích thích như GM-CSF, G-CSF, IL-3.
Sô lượng CD34+ nhiều, cao hơn scí lượng ở tuỷ.
Khả năng sinh sản lớn gấp 4 - 5 có khi tối 10 so vói tế bào tuỷ
Tế bào có thẩm quyền miễn dịch (T lympho) ít, hoạt tính của T-CD8 rất thấp do đó GVHD yếu.
Nhiều progenitor: BFU-E, CFU-E, CFU-Meg, CFU-GEMM, CFU-GM.
Thu hoạch
Máu cuống ròn chống đông ACD - hỗn hợp với heparin theo tỷ lệ 10Ư heparin/ml ACD.
Tách bằng máy tự động, hoặc
Tách bằng ly tâm phân lớp.
Đánh giá sô lượng CD34 bằng phương pháp huỳnh quang và scí lượng GM / CFU bằng phương pháp nuôi cấy clon.
Bảo quản lạnh sâu (như trên).
Xây dụng ngân hàng tế bào nguồn máu rốn
Tách CD34.
Loại T.
Định HLA.
Bảo quản lạnh: bảo quản trong nitơ lỏng (liquid nitrogen) đạt được âm 196°c, có thể giữ được 4 - 5 năm trong điều kiện này.
Phương pháp ghép tuỷ tế bào nguồn
Ghép tuỷ tế bào nguồn, nghĩa là truyền tế bào nguồn vào máu như truyền máu, nhưng không dùng màng lọc máu, truyền chậm và dùng kim luồn vào tĩnh mạch trung tâm.
Bệnh có thể ghép tủy
Bệnh ung thư lỏng: All, AML, CLL CML, Hodgkin, nonHodgkin, myeloma.
Ung thư cứng: ung thư vú, tử cung, phổi.
Suy tuỷ, rối loạn sinh tuỷ (MDS).
Di truyền: Thalassemia, Glanzmann...
Suy giảm miễn dịch: AIDS, lupus.
Ghép tủy đống loài
Để ghép tủy đồng loài có kết quả, cần có hai điều kiện tối quan trọng đó là:
Tương đồng: ABO, HLA phải có ít nhất ba gen giông nhau, ít hơn thì khả năng đậu ghép rất khó khăn do bệnh ghép chống chủ gây nên.
Phòng bệnh ghép chống chủ, phòng thải ghép.
Tiến hành ghép tủy theo ba bước sau đây:
Chuẩn bị bệnh nhân:
Dùng hóa chất liều cao để tiêu diệt tế bào miễn dịch của cơ thể nhân. Thông thường có thể dùng một trong hai phương pháp:
Hoá chất đơn:
Cyclophosphamid : 120 mg/kg.
Etoposid: 60 mg/kg.
Melphalan: 110 mg/kg.
Đa hoá chất:
Cytosa + cyclophosphamid : 3g/kg + 50 - 120mg/kg.
Busulphan + cyclophosphamid: 7mg/kg + 50 mg/kg.
Etoposid + cyclophosphamid : 30 -60kg + 1500 mg/kg.
Hoá chất phối hợp với ATG:
Cyclophosphamid 200mg/kg.
ATG = 90 mg/kg.
Hóa chất phối hợp với tia xạ toàn thân (TBI) để tiêu diệt tối đa tế bào miễn dịch.
Ghép tủy
Truyền tế bào nguồn vào tĩnh mạch trung tâm qua kim luồn catheter.
Chăm sóc sau ghép tủy
Phòng bệnh ghép chống túc chủ (GVHD):
Đây là phản ứng nguy hiểm nhất của ghép tủy đồng loài; Phòng GVHD bằng các thuốc sau đây:
Cyclosporin A.
Methotrexat.
Prednisolon.
ATG.
Điều trị hỗ trợ:
Chống nhiễm trùng, nấm: kháng sinh dự phòng, có phòng chăm sóc vô trùng.
Sử dụng hợp lý máu và các sản phẩm máu.
Chỉ định hợp lý máu và các sản phẩm máu.
Chế độ dinh dưỡng tốt, an toàn.
Sử dụng các íactor phát triển: GM-CSF, G-CSF.
Đánh giá kết quả
Theo dõi giám sát:
Theo dõi bệnh ghép chống chủ.
Nuôi cấy GM-CFU theo dõi tế bào ghép phát triển.
Xét nghiệm máu: hồng cầu, tiểu cầu.
Xét nghiệm sớm các nguy cơ dẫn đến không kết quả.
Tái phát (Relapse).
Nhiễm trùng: thường gặp nhiễm virus (CMV, Herpes EBV) nhiễm nấm, nhiễm trùng Gram (+), Gram (-).
Phát hiện các yếu tố dẫn đến kết quả xấu:
Bệnh không đông máu.
HLA không quan hệ huyết thống...
Úc chế miễn dịch không đầy đủ.
Tế bào T còn cao.
Sống tự do 3-5 năm cần dùng hoá chất ức chế phản ứng MD từng đợt:
Busulphan 16 mg/kg/ngày X 4 ngày.
Dùng tiếp cyclophosphamid 120 mg/kg/ngày X 2 ngày.
Phát hiện bệnh ghép chống chủ (GVHD)
Biểu hiện của bệnh ghép chống chủ cấp:
Bệnh thường xuất hiện sau khi ghép từ ngày 10 - 12, triệu chứng nổi bật là da, bệnh gút, bệnh gan, phổi và bệnh hệ miễn dịch.
Các biểu hiện ở da: rát đỏ, nốt phồng đỏ ở gan bàn tay, bàn chân, nách, cơ vai, mặt trong các cơ gấp...
Biểu hiện ở đường chuyển hoá: thường tổn thương gan làm bilirubin tăng, men gan tăng, tổn thương tế bào biểu mô đường tiêu hoá. Do đó dẫn đến rối loạn chuyển hóa các chất.
Bệnh gút: đau, buốt các đầu ngón chân...
Xét nghiệm tế bào T-CD4+ và T-CD8+, các cytokin IL-2, INF... các cytokin này sẽ làm tăng quá trình tổn thương tổ chức.
Biểu hiện của GVHD mạn:
Ghép đồng loài chọn lọc HLA có tới 20-30%, có tác giả thông báo 60% có GVHD mạn... Nguyên nhân chính vẫn là do tế bào T lympho của tế bào ghép chưa được làm sạch. Thường 40 ngày sau, có khi sau 1 năm mối xuất hiện. Các biểu hiện lâm sàng vẫn chủ yếu ở da và bệnh gan. Gan có thể bị xơ gan, viêm gam mạn tiến triển, tổn thương mắt, niêm mạc.
Ngoài ra bệnh ghép chống chủ còn biểu hiện ở thận như hội chứng tan máu sau ghép, đái máu,... Bệnh ở phổi với các biểu hiện viêm phổi,... bệnh nội tiết, thường có hội chứng tăng nội tiết tố, biểu hiện lâm sàng rất ít, khám nội tiết có thể gặp 50 - 60% các trường hợp, đục nhân mắt (cataracts) gặp 10 - 20%, bệnh xương thường gặp là loãng xương, bệnh ung thư thứ phát thường do hậu quả của các virus tấn công vào cơ thể nhất là EBV gây u lympho.
Phòng và điều trị bệnh ghép chống chủ
Dự phòng:
Loại T lympho khỏi tế bào nguồn ghép
Úc chế phân bào T lympho:
Prednisolcn
Cyclosporin A + ATG
Điểu trị:
Dùng các thuốc chống phân bào T lympho, kèm theo chăm sóc sốt, nhiễm trùng, chăm sóc chức phận gan thận.
Tiên lượng GVHD: nhìn chung nếu GVHD xuất hiện thì tiên lượng rất xấu.
Ghép tủy tự thân
Dùng tế bào nguồn của bệnh thép lại cho bệnh nhân. Trường hợp này không cần lựa chọn HLA. Nhưng vấn đề loại bỏ tế bào ung thư lại trở nên cần thiết. Công việc được tiến hành theo các bước sau đây:
Chuẩn bị tế bào nguồn
Thu hoạch tế bào CD34 từ máu:
Huy động tế bào nguồn: sau điều trị hóa chất tế bào leukemia bị tiêu diệt, tiến hành tiêm G-CSF, sau đó thu hoạch tế bào nguồn
Làm sạch tếbào ung thư (tếbào lơxêmi) bằng hai cách:
Sử dụng kháng thể đơn dòng đặc hiệu lơxêmi, diệt tế bào ung thư trước khi truyền.
Tạo kháng thể chống lơxêmi ngay trong bản thân bệnh nhân tự ghép. Tế bào ung thư còn lẫn trong huyền dịch tế bào gốíc nhưng đã bị bất hoạt bởi kháng thể đặc hiệu khi truyền vào cơ thể nhận, chúng trở thành kháng nguyên lạ với cơ thể, cơ thể có khả năng đáp ứng miễn dịch, tạo kháng thể chổng tế bào leukemia. Đó là hình thức loại bỏ tế bào ung thư.
Đông lạnh tế bào nguồn cũng có tác dụng loại bỏ tế bào leukemia (tế bào leukemia dễ chết).
Bảo quản: đông lạnh ở nhiệt độ - 180°c, hoặc truyền ngay sau bảo quản ở 4°c trong 3 ngày.
Chuẩn bị bệnh nhân và ghép tủy
Hóa trị liệu liều cao: Tiêu diệt triệt để tế bào ung thư sử dụng các thuốc: cyclophosphamid; caromustin; melfalan; etoposid; cytosin-arabinosid; thioguanin.
Tia xạ liều toàn thân (TBI).
Ghép tủy: Truyền tế bào tủy (tế bào CD34+) vào tĩnh mạch trung tâm đã đặt trước catheter.
Làm tan đông rất nhanh.
Truyền tủy.
Tai biên có thể có khi truyền tủy: buồn nôn, nôn, đau bụng, khó thở, tăng HA, rôi loạn chức phận thận do các thành phần tế bào đông tan giải phóng ra.
Chăm sóc sau ghép tủy
Hô trợ: các sản phẩm máu, kháng sinh chống nhiễm trùng, dinh dưỡng, các factor phát triển.
Theo dõi sự phát triển của tế bào tuỷ ghép.
Bài viết cùng chuyên mục
Các bệnh truyền nhiễm qua đường truyền máu và an toàn truyền máu
HIV có tỷ lệ biến dị khá lớn, trong quá trình sao chép nếu có sự thay đổi một ví trí nào đó của các nucleotid là có thể tạo ra một virus mới khác với virus nguyên bản. Các virus mới sẽ ẩn náu trong các tế bào của cơ thể và trở thành kháng thuốc.
Truyền máu tự thân và ứng dụng
Phải kiểm tra các thành phần bạch cầu, hồng cầu ly giải trong đơn vị máu, tuy nó không có nguy hại lớn về lâm sàng như truyền máu đồng loài, nhưng khi có hàm lượng cao thì truyền cho người bệnh cũng có thể xảy ra tai biến.
Cấu trúc và chức năng huyết sắc tố (Hb)
Huyết sắc tố còn gọi là hemoglobin (Hb) là một protein phức có chứa Fe++, làm nhiệm vụ vận chuyển oxy từ phổi đến tổ chức và vận chuyển CO2, từ tổ chức về phổi, Hb ở trong hồng cầu và chiếm 33% trọng lượng hồng cầu.
Các cytokin và điều hòa tạo máu
Các cytokin có tác dụng điều hoà hoạt động và phát triển tế bào đích, do đó chúng đang được sử dụng trên lâm sàng để điều trị bệnh nhất là bệnh suy giảm miễn dịch.
Bất thường vật chất di truyền và bệnh máu
Có thể phân chia bất thường vật chất di truyền theo nguyên nhân bẩm sinh hay măc phải, hoặc phân chia theo mức độ tổn thương: bất thường mức độ nhiễm sắc thể và mức độ gen.
Bệnh lupus ban đỏ hệ thống (Systemic Lupus Erythematosus - SLE)
Triệu chứng lâm sàng biểu hiện trên nhiều tạng trong cơ thể bệnh nhân, nhưng thường gặp nhiều hơn là sốt, triệu chứng ở da, triệu chứng cơ - khớp, triệu chứng về huyết học, thận và tim mạch.
Hệ nhóm máu ABO, Rh, các hệ khác và an toàn truyền máu
Các kháng nguyên nhóm máu, là các sản phẩm protein trên màng hồng cầu, mà quá trình tổng hợp, những protein này được mã hóa.
Bệnh xuất huyết giảm tiểu cầu
Giảm tiểu cầu miễn dịch ở trẻ sơ sinh là do bất đồng kháng nguyên HPA giữa mẹ và con, gây miễn dịch ở mẹ và giảm tiểu cầu ở con. Hầu hết các trường hợp được chẩn đoán sau đẻ.
Miễn dịch cơ bản trong huyết học truyền máu
Miễn dịch không đặc hiệu là miễn dịch không do phản ứng kháng nguyên- kháng thể như hiện tượng thực bào của bạch cầu, các dịch tiết của mắt, đường tiêu hoá.
Lơ xê mi kinh dòng hạt
Lơ xê mi kinh dòng hạt là một bệnh ác tính hệ tạo máu, đặc trưng bởi sự tăng sinh các tế bào dòng bạch cầu hạt biệt hóa, hậu quả là số lượng bạch cầu tăng cao ở máu ngoại vi với đủ các tuổi của dòng bạch cầu hạt.
Kỹ thuật tế bào và sinh hóa phân tử trong nghiên cứu bệnh máu
Sử dụng các men hạn chế cắt ADN tại các vị trí đặc hiệu, sau đó điện di và so sánh độ dài của đoạn ADN giữa hai vị trí cắt, Kỹ thuật này có thể giúp phát hiện các thểm đoạn, mất đoạn gen hay phát hiện đột biến điểm tại vị trí men bình thường chọn cắt.
Đa hồng cầu nguyên phát (polycythaemia vera)
Sinh thiết tủy xương. tủy giàu tế bào, tăng sinh ba dòng tế bào đặc biệt là tăng sinh và loạn sản dòng mẫu tiểu cầu, đôi khi kèm theo xơ hoá tủy.
Phân loại và chẩn đoán hội chứng tăng sinh tủy mạn ác tính
Tuỷ đồ chẩn đoán tế bào học, Sinh thiết: chẩn đoán tổ chức tuỷ, Các xét nghiệm đặc trưng riêng cho từng bệnh.
Phân loại chẩn đoán bệnh lý tế bào nguồn ngoài tủy
Nội tiết tố, chất kích thích phát triển, muối khoáng, do đó bệnh lý máu ngoại vi có thể chia 2 nhóm như sau, Nhóm bệnh lý tế bào, nhóm bệnh lý huyết tương.
Xơ tủy nguyên phát (myelofibrosis)
Nhìn chung ban đầu bệnh có biểu hiện là tăng sinh ở tủy xương với tăng số lượng tế bào, sau đó là giảm sinh tủy với giảm ba dòng tế bào máu ngoại vi.
Lịch sử phát triển truyền máu thế giới
Công trình khoa học có giá trị nhất, lợi ích nhất trong truyền máu là sự phát minh ra các kháng nguyên hệ hồng cầu và nhóm máu của Karl Landsteiner.
Đảm bảo chất lượng trong xét nghiệm huyết học truyền máu
Công tác truyền máu được đảm bảo chất lượng có nghĩa là máu và thành phẩm truyền cho bệnh nhân đáp ứng tốt nhất nhu cầu điều trị và hạn chế đến mức thấp nhất các kết quả không mong muốn.
Nguồn gốc phát triển, cấu trúc và chức năng của tiểu cầu
Bình thường tiểu cầu không dính vào thành mạch, có lẽ do một chất có tác dụng ức chế dính của tiểu cầu - chất đó có thể là prostaglandin. Tuy nhiên khi có đứt mạch máu thì lập tức tiểu cầu được hoạt hóa và dính vào nơi tổn thương.
Các tiến bộ về huyết học truyền máu
Gây nhiều phản ứng khi truyền máu do có các chất trung gian và hậu quả sau truyền máu do kháng nguyên HLA và HPA.
Thiếu máu tan máu miễn dịch
Hiệu giá kháng thể miễn dịch rất thay đổi tăng lên rõ rệt ở môi trường albumin, còn hiệu giá kháng thể tự nhiên tăng lên rõ rệt ở môi trường muối.
Phân bố gen và chức năng của HLA trong cơ thể
HLA lớp I và II hợp tác trong quá trình miễn dịch bao gồm cả trả lời miễn dịch và phản ứng kháng nguyên- kháng thể của cả miễn dịch tế bào.
Phân loại bệnh lý tế bào nguồn sinh máu và bệnh máu
Tuy phân làm hai nhóm, nhưng cả hai liên quan và gắn bó với nhau rất chặt chẽ như bệnh lý của tuỷ xương lại được phản ánh ở máu ngoại vi và số lượng và hình ảnh máu ngoại vi cũng phản ánh bệnh lý của tuỷ xương.
Quá trình sinh máu bình thường
Trong quá trình phát triển, tế bào nguồn sinh máu có khả năng sinh sản và biệt hoá thành các tế bào máu trưởng thành có chức năng riêng biệt, Người ta chia tế bào nguồn sinh máu thành bốn loại.
Lâm sàng và xét nghiệm thiếu máu tan máu
Thay đổi cấu trúc xương do tủy xương tăng cường hoạt động, thường chỉ gặp ở trẻ em, đang lúc tuổi phát triển. Hố tủy xương giãn rộng, xương sọ có hình bàn chải.
Tăng đông và huyết khối
Một số tác giả gọi tăng đông là tình trạng tiền huyết khối. Tuy nhiên cần lưu ý răng huyêt khối thường ít khi do một nguyên nhân đơn độc gây nên mà thường là hậu quả của sự kết hợp của một số những rối loạn và yếu tố nguy cơ.
